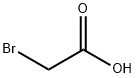
| Хімічні властивості |
КРИСТАЛІЧНА МАСА ВІД БІЛОГО ДО СВІТЛО-ЖОВТОГО |
| Використання |
Органічний синтез, осипання плодів цитрусових при збиранні. |
| Використання |
Бромоцтова кислота використовується в органічному синтезі і як алкілуючий агент. Він також використовується як біохімічний засіб для дослідження протеоміки. Це важлива сировина та проміжний продукт, який використовується в органічному синтезі, фармацевтиці, барвниках та агрохімікатах. |
| Використання |
Бромоцтова кислота в основному використовується дляN-кінцеве бромоацилювання пов'язаних зі смолою пептидів.
Його також можна використовувати:Синтезувати (Z)-2-(циклоокт-4-ен-1-ілокси)оцтова кислота.
Синтезувати -бромфенілацетамід.
Для перетворення ароматичних тіосемікарбазонів у тіазолілгідразони.
|
| Загальний опис |
Водний розчин. |
| Реакції повітря та води |
Розчинний у воді. |
| Профіль реактивності |
Карбонові кислоти, такі як БРОМУЦТОВА КИСЛОТА, віддають іони водню, якщо присутня основа для їх прийняття. Таким чином вони реагують з усіма основами, як органічними (наприклад, аміни), так і неорганічними. Їх реакції з основами, які називаються «нейтралізаціями», супроводжуються виділенням значної кількості тепла. Нейтралізація між кислотою та основою дає воду та сіль. Карбонові кислоти з шістьма або меншими атомами вуглецю вільно або помірно розчинні у воді; ті, що містять більше шести атомів вуглецю, малорозчинні у воді. Розчинна карбонова кислота певною мірою дисоціює у воді з утворенням іонів водню. Таким чином, рН розчинів карбонових кислот менше ніж 7.0. Багато нерозчинних карбонових кислот швидко реагують з водними розчинами, що містять хімічну основу, і розчиняються, коли в результаті нейтралізації утворюється розчинна сіль. Карбонові кислоти у водному розчині та рідкі або розплавлені карбонові кислоти можуть реагувати з активними металами з утворенням газоподібного водню та солі металу. Такі реакції відбуваються в принципі і для твердих карбонових кислот, але вони повільні, якщо тверда кислота залишається сухою. Навіть «нерозчинні» карбонові кислоти можуть поглинати достатню кількість води з повітря та достатньо розчинятися в бромоцтовій кислоті, щоб викликати корозію або розчинити залізні, сталеві та алюмінієві деталі та контейнери. Карбонові кислоти, як і інші кислоти, реагують з ціаністими солями з утворенням газоподібного ціаністого водню. Реакція відбувається повільніше для сухих твердих карбонових кислот. Нерозчинні карбонові кислоти реагують з розчинами ціанідів, викликаючи виділення газоподібного ціаністого водню. Займисті та/або токсичні гази та тепло утворюються в результаті реакції карбонових кислот з діазосполуками, дитіокарбаматами, ізоціанатами, меркаптанами, нітридами та сульфідами. Карбонові кислоти, особливо у водному розчині, також реагують із сульфітами, нітритами, тіосульфатами (утворюючи H2S і SO3), дитіонітами (SO2), утворюючи легкозаймисті та/або токсичні гази та тепло. Їх реакція з карбонатами та бікарбонатами генерує нешкідливий газ (вуглекислий газ), але все ще нагрівається. Як і інші органічні сполуки, карбонові кислоти можуть окислюватися сильними окислювачами і відновлюватися сильними відновниками. Ці реакції генерують тепло. Можливий широкий асортимент продукції. Як і інші кислоти, карбонові кислоти можуть ініціювати реакції полімеризації; як і інші кислоти, вони часто каталізують (збільшують швидкість) хімічні реакції. |
| Небезпека |
Сильний подразник шкіри та тканин. |
| Небезпека для здоров'я |
ТОКСИЧНИЙ; вдихання, проковтування або контакт (шкіра, очі) з парами, пилом або речовиною може призвести до серйозних травм, опіків або смерті. Контакт з розплавленою речовиною може спричинити серйозні опіки шкіри та очей. Реакція з водою або вологим повітрям призведе до виділення токсичних, корозійних або легкозаймистих газів. Реакція з водою може генерувати багато тепла, що збільшить концентрацію парів у повітрі. Вогонь вироблятиме дратівливі, корозійні та/або токсичні гази. Стік від пожежогасіння або води для розведення може бути корозійним та/або токсичним і спричиняти забруднення. |
| Небезпека пожежі |
Горючий матеріал: може горіти, але не легко запалюється. Речовина реагує з водою (деякі бурхливо), вивільняючи легкозаймисті, токсичні або корозійні гази та стікання. При нагріванні пари можуть утворювати вибухонебезпечні суміші з повітрям: небезпека вибуху в приміщенні, на вулиці та в каналізації. Більшість парів важчі за повітря. Вони поширюються по землі та збираються в низинних або обмежених місцях (каналізація, підвали, резервуари). Пари можуть потрапити до джерела займання та спалахнути назад. При контакті з металами можливе виділення горючого водню. Контейнери можуть вибухнути при нагріванні або забрудненні водою. |
| Займистість і вибухонебезпечність |
Негорючий |
| Профіль безпеки |
Отрута при ковтанні, внутрішньоочеревинному та внутрішньовенному введенні. Подразнює та роз'їдає шкіру та слизові оболонки. Повідомлено дані про мутації. При нагріванні до розкладання виділяє токсичні пари Br-. Дивіться також БРОМІДИ. |
| Методи очищення |
Викристалізуйте бромооцтову кислоту з петролейного ефіру (b 40-60o). Розчин його в діетиловому ефірі пропускають через колонку з оксидом алюмінію і ефір випаровують при кімнатній температурі під вакуумом. Його найкраще отримувати дистиляцією з Клайзена (колба, занурена в масляну баню), оснащеного ізольованою колонкою Вігре (стор. 11), і збирають фракцію b 108-110o/30 мм. Він чутливий до світла та вологи. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] СЛИЗОВИХОДНИЙ і є ДРАЖНИКОМ шкіри. |