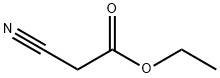
| опис |
Етилціаноацетат - це етиловий ефір ціанооцтової кислоти. Етилціаноацетат швидко гідролізується в нейтральних і лужних умовах до ціанооцтової кислоти та етанолу (і так відбувається в більшості фізіологічних умов і умов навколишнього середовища), тоді як при кислому рН період напіврозпаду значно довший.
Повідомляється про конденсацію етилціаноацетату з альдегідом за Кневенагелем. Повідомляється про реакцію конденсації етилціаноацетату за Кноевенегалем, посилену мікрохвилями, з альдегідом, P2O5, піперидином і хлорбензолом. |
| Хімічні властивості |
Етилціаноацетат — рідина від безбарвного до солом’яного кольору з легким приємним запахом |
| Використання |
Етилціаноацетат може бути використаний у синтезі етилгліоксилату. Його використовували для дослідження реакцій конденсації Кневенагеля в мікрореакторі з використанням цеолітних каталізаторів, отриманих шляхом щеплення аміногруп до цеолітів NaX і CsNaX. |
| Використання |
Реагент, який використовується для синтезу міченого піримідину та пурину. Етилціаноацетат є складним ефіром. Він може бути використаний у синтезі етилгліоксилату. Його використовували для дослідження реакцій конденсації Кневенагеля в мікрореакторі з використанням цеолітних каталізаторів, отриманих шляхом щеплення аміногруп до цеолітів NaX і CsNaX. |
| Підготовка |
Етилціаноацетат можна одержати дією ціаніду натрію або калію на етилхлорацетат і дією ціаніду натрію на хлорацетат натрію з наступною етерифікацією. |
| Загальний опис |
Безбарвна рідина. Щільніше води. Контакт може викликати подразнення шкіри, очей і слизових оболонок. Температура спалаху 210 градусів F. Може бути токсичним при проковтуванні. Використовується для виготовлення інших хімікатів. |
| Реакції повітря та води |
Малорозчинний у воді. |
| Профіль реактивності |
Етилціаноацетат є як нітрилом, так і складним ефіром. Складні ефіри реагують з кислотами з виділенням тепла разом зі спиртами та кислотами. Сильні окислювачі кислоти можуть викликати бурхливу реакцію, яка є достатньо екзотермічною, щоб запалити продукти реакції. Тепло також виділяється при взаємодії складних ефірів з їдкими розчинами. Легкозаймистий водень утворюється шляхом змішування складних ефірів з лужними металами та гідридами. Нітрили можуть полімеризуватися в присутності металів і деяких сполук металів. Вони несумісні з кислотами; змішування нітрилів із сильними кислотами-окислювачами може призвести до надзвичайно бурхливих реакцій. Нітрили, як правило, несумісні з іншими окислювачами, такими як пероксиди та епоксиди. Поєднання основ і нітрилів може утворювати ціаністий водень. Нітрили гідролізуються як у водному розчині кислоти, так і в основі з утворенням карбонових кислот (або солей карбонових кислот). Ці реакції генерують тепло. Пероксиди перетворюють нітрили в аміди. Нітрили можуть активно реагувати з відновниками. Ацетонітрил і пропіонітрил розчиняються у воді, але нітрили, вищі за пропіонітрил, мають низьку розчинність у воді. Вони також нерозчинні у водних кислотах. |
| Небезпека |
Токсичний при ковтанні та вдиханні. |
| Небезпека для здоров'я |
ТОКСИЧНИЙ; вдихання, проковтування або контакт (шкіра, очі) з парами, пилом або речовиною може призвести до серйозних травм, опіків або смерті. Контакт з розплавленою речовиною може спричинити серйозні опіки шкіри та очей. Реакція з водою або вологим повітрям призведе до виділення токсичних, корозійних або легкозаймистих газів. Реакція з водою може генерувати багато тепла, що збільшить концентрацію парів у повітрі. Вогонь вироблятиме дратівливі, корозійні та/або токсичні гази. Стік від пожежогасіння або води для розведення може бути корозійним та/або токсичним і викликати забруднення. |
| Небезпека пожежі |
Горючий матеріал: може горіти, але не легко запалюється. Речовина реагує з водою (деякі бурхливо), вивільняючи легкозаймисті, токсичні або корозійні гази та стікання. При нагріванні пари можуть утворювати вибухонебезпечні суміші з повітрям: небезпека вибуху в приміщенні, на вулиці та в каналізації. Більшість парів важчі за повітря. Вони поширюються по землі та збираються в низинних або обмежених місцях (каналізація, підвали, резервуари). Пари можуть потрапити до джерела займання та спалахнути назад. При контакті з металами можливе виділення горючого водню. Контейнери можуть вибухнути при нагріванні або забрудненні водою. |
| Профіль безпеки |
отруєння шляхом проковтування. Помірно токсичний при внутрішньоочеревинному та підшкірному введенні. Горить під впливом тепла або полум'я; може реагувати з окисними матеріалами. Wdl реагує з водою або парою з утворенням токсичних і легкозаймистих парів. Для гасіння пожежі використовуйте CO2, сухий хімікат. При нагріванні до розкладання або при контакті з кислотою або кислотними парами він виділяє високотоксичні пари CN-. Дивіться також НІТРИЛИ. |
| Потенційний контакт |
Нітрил, який використовується для виробництва барвників, фармацевтичних препаратів та інших хімікатів. |
| Перша допомога |
Якщо ця хімічна речовина потрапила в очі, негайно зніміть будь-які контактні лінзи та негайно зрошуйте їх протягом принаймні 15 хвилин, час від часу піднімаючи верхню та нижню повіку. Негайно зверніться до лікаря. Якщо ця хімічна речовина потрапить на шкіру, зніміть забруднений одяг і негайно вимийтеся водою з милом. Негайно зверніться до лікаря. Якщо цю хімічну речовину вдихнули, усуньте її від впливу, почніть рятувальне дихання (використовуючи універсальні запобіжні заходи, включаючи реанімаційну маску), якщо дихання зупинилося, і СЛР, якщо серцева діяльність зупинилася. Негайно доставити до медичного закладу. Якщо цю хімічну речовину проковтнули, зверніться за медичною допомогою. Дати велику кількість води та викликати блювоту. Не викликайте блювоту у непритомної людини |
| зберігання |
повторне розташування отрути. Перед початком роботи з цим хімікатом ви повинні пройти навчання щодо його правильного поводження та зберігання. Зберігайте в щільно закритих контейнерах у прохолодному, добре провітрюваному місці подалі від окислювачів, сильних лугів, сильних кислот, відновників, вологи та джерел займання. Якщо можливо, автоматично перекачуйте рідину з бочок або інших контейнерів для зберігання в контейнери для обробки |
| Доставка |
UN3276 Нітрили, рідкі, токсичні, н.у., клас небезпеки: 6.1; Мітки: 6.1-Отруйні матеріали, необхідна технічна назва, потенційна небезпека при вдиханні (Спеціальне положення 5). |
| Методи очищення |
Естер кілька разів збовтують з 10% водним розчином Na2CO3, добре промивають водою, висушують Na2SO4 і дробно переганяють. [Beilstein 2 IV 1889.] |
| Несумісність |
Несумісний з окислювачами (хлорати, нітрати, пероксиди, перманганати, перхлорати, хлор, бром, фтор та ін.); контакт може спричинити пожежу або вибух. Тримайте подалі від лужних матеріалів, сильних основ, сильних кислот, оксокислот, епоксидів і відновників. Нітрили можуть полімеризуватися в присутності металів і деяких сполук металів. Вони несумісні з кислотами; змішування нітрилів із сильними кислотами-окислювачами може призвести до надзвичайно бурхливих реакцій. Нітрили, як правило, несумісні з іншими окислювачами, такими як пероксиди та епоксиди. Поєднання основ і нітрилів може утворювати ціаністий водень. Нітрили гідролізуються як у водному розчині кислоти, так і в основі з утворенням карбонових кислот (або солей карбонових кислот). Ці реакції генерують тепло. Пероксиди перетворюють нітрили в аміди. Нітрили можуть активно реагувати з відновниками. Ацетонітрил і пропіонітрил розчиняються у воді, але нітрили, вищі за пропіонітрил, мають низьку розчинність у воді. Вони також нерозчинні у водних кислотах. Реагує з вологою, водою та парою, утворюючи токсичні пари. |
| Утилізація відходів |
Проконсультуйтеся з екологічними регуляторними органами, щоб отримати вказівки щодо прийнятної практики утилізації. Виробники відходів, що містять цей забруднювач (більше або дорівнює 100 кг/міс), повинні відповідати правилам EPA щодо зберігання, транспортування, обробки та утилізації відходів. |